Étude SEAMLESS (ENGOT en-21)
Fiche descriptive de l'étude
Étude Utérus
Étude SEAMLESS/ENGOT en-21 - Cancer Endomètre avancé ou rechute
Titre de l'étude
SEAMLESS (ENGOT en-21) : Etude de phase 2/3 utilisant le Navtemadlin en entretien chez des patientes atteintes de cancer d’endomètre avancé ou récidivant TP53WT ayant répondu à la chimiothérapie
Statut
En cours de recrutement
Plan de traitemement de l'étude
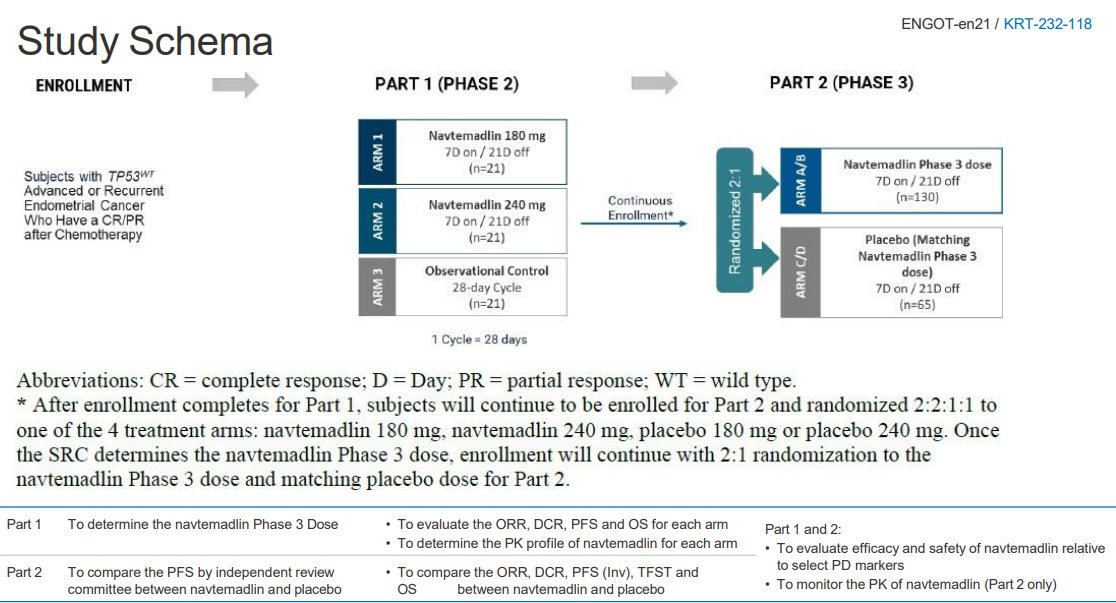
Promoteur
Kartos Therapeutics, Inc
But
Objectifs primaires :
- Pour la partie 1 : Déterminer la dose du navtemadlin pour la phase 3.
- Pour la partie 2 : Comparer la survie sans progression (PFS) entre la navtemadlin et le placebo par un comité indépendant (IRC)
Objectifs secondaires :
Pour la partie 1 : Evaluation de l'effet du navtemadlin sur la PFS par un comité indépendnat (IRC) et l'évaluation de l'investigateur.
Note Le TFST : est le délai entre la randomisation et le début du traitement à la rechute ou le décès.
Pour les parties 1 et 2
- Evaluation de l'effet du navtemadlin sur la survie globale (OS).
- Evaluation de l'effet du navtemadlin sur le taux de réponse objective (ORR).
- Evaluation de l'effet du navtemadlin sur le taux de contrôle de la maladie (DCR).
- Identification du profil pharmacocinétique (PK) du navtemadlin.
- Evaluation de la safety et tolérabilité du navtemadlin.
Critère principaux d’évaluation
- Pour la partie 1: Les données de sécurité de la phase 1 vont permettre d’évaluer la dose du navtemadlin pour la phase 3.
- Pour la partie 2: la PFS est le délai entre la randomisation et la progression de la maladie ou le décès, définie par un comité indépendant (IRC).
Phase
Phase II/III
Type de patiente
Femmes âgées de 18 ans ou plus atteintes d'un cancer de l'endomètre TP53WT avancé ou récurrent et présentant une RC ou une RP après 6 cycles de chimiothérapie.
Nombre de patientes recrutées (en cours de lancement) :
00 patientes dans environ 00 centres
00 patientes en France dans 11 centres







