Le cas des cancers du sein ou de l'ovaire
La génétique oncologique
C'est une discipline récente. L’identification et le clonage des gènes BRCA1 et BRCA2 dans les années 1990s ont poser les bases moléculaires des syndromes de prédisposition au cancer du sein.
Initialement focalisées aux gènes BRCA1 et BRCA2, les analyses ont ensuite été étendues dans le courant des années 2010 à d’autres gènes. Actuellement, une recherche de prédisposition aux cancers du sein se réalise selon un panel de 13 gènes (BRCA1, BRCA2, PALB2, CDH1, TP53, PTEN, RAD51C, RAD51D, MLH1, MSH2, MSH6, PMS2, EPCAM), impliqués dans les formes héréditaires de cancer du sein et/ou de l’ovaire. D’autres gènes sont en cours d’évaluation (CHEK2 ou ATM). L'objectif est de pouvoir caractériser et définir une prise en charge adaptée.
Les prédispositions génétiques aux cancers gynécologiques
Organes cibles : seins ovaires
- Syndrome seins-ovaires : mutation constitutionnelle délétère (MCD) de BRCA1 ou BRCA2
- Transmission autosomique dominante
Organes cibles : endomètre ovaires
- Syndrome de Lynch : mutation constitutionnelle d’un gène de système de réparation des mésappariements de l’ADN : gènes MMR
- Transmission autosomique dominante
Le syndrome sein/ovaires
Chez approximativement une personne sur 500, l’un des gènes BRCA1, BRCA2 ou PALB2 est altéré et est à l’origine, chez ces femmes, d’une prédisposition génétique majeure aux cancers du sein et de l’ovaire.
Le risque de cancer du sein, cumulé au cours de la vie, est important ; il s’agit souvent de cancers de survenue précoce chez l’adulte jeune.
- En cas de mutation de BRCA1, à l’âge de 70 ans, les risques cumulés de cancer du sein et de l’ovaire sont respectivement, de l’ordre de 65-80 % et de 40 %
- En cas de mutation portant sur le gène BRCA2, les risques cumulés sont moindre, 45-60 % pour le sein et 10-40 % pour l'ovaire.
- Le risque de cancer de l'ovaire en cas de mutation BRCA2 varie en fonction de la localisation de la mutation sur le gène : il est majeur dans la région centrogénique (OCCR pour ovarian cancer cluster region)
- Depuis 2017, le gène PALB2 fait partie des gènes devant être étudiés face à un risque héréditaire du cancer du sein. La surveillance mammaire chez une patiente mutée PALB2 doit comporter, en plus de l’examen clinique, une IRM couplée à une mammographie et éventuellement une échographie de manière annuelle, de 30 à 65 ans.
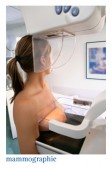
Suivi d'une personne prédisposée à développer un cancer du sein
LE CONTEXTE
Quelques chiffres
On estime qu'environ 5 % des cancers du sein ont une prédisposition génétique, alors que 20 % ont une histoire familiale. En France, cela représente 2 000 nouveaux cas de cancers du sein et 200 cancers de l’ovaire.
Quelle(s) mutation(s)
Des études récentes ont montré que la plupart de ces cancers sont dus à des mutations héréditaires de certains gènes.
Dans 20 à 40 % des cas, il s'agit du gène BRCA1 , cloné en 1994 et porté par le chromosome13q12-13.
Dans 10 à 30 % des cas, le gène en cause est le BRCA2 porté par le chromosome 17q12-21, cloné en 1995.
Les tumeurs sont des carcinomes canalaires infiltrants
Elles sont de grade élevé (85 % de grade III), avec un important infiltrat lymphocytaire et des foyers de nécrose.
Plus de 80 % des tumeurs ayant pour origine des mutations de BRCA1 sont de phénotype triple-négatif (n’exprimant ni récepteurs des œstrogènes ni récepteur de la progestérone et ne présentant pas d’amplification du récepteur Her2-neu (Human Epidermal growth factor Receptor 2).
LES RECOMMANDATIONS ACTUELLES
Le contexte
La présence de cette altération chez une femme accroît le risque de développer :
- Un cancer du sein à un âge précoce (âge moyen de diagnostic : 44 ans)
- Un cancer sur le sein controlatéral après diagnostic d’un premier cancer
- Un cancer de l’ovaire, essentiellement après 40 ans, le risque variant dans ce cas selon le gène touché et l’histoire familiale associée
Le suivi
Dans le cas général il comporte :
- Dès 25 ans, tous les 6 mois, un examen clinique des seins tous les 6 mois
- Dès 30 ans, tous les ans, une mammographie bilatérale avec échographie et une échographie pelvienne pour vérifier les ovaires ; l'IRM est une option alternative à la mammographie.
Quelle prophylaxie ?
Une annexectomie (ablation des ovaires) est recommandée chez les femmes porteuses d'une mutation BRCA1 , à partir de 40 ans ou ayant le nombre d'enfants souhaité.
Une mammectomie de prévention n'est pas recommandée, en général. Elle demeure optionnelle chez les femmes porteuses de la mutation. Dans ce cas, après demande de la patiente et une évaluation psychologique, la décision est prise en réunion de concertation pluridisciplinaire (RCP).
La mise en œuvre d'une hormonothérapie par tamoxifène ou inhibiteurs de l'aromatase est du domaine de la recherche clinique.
Génétique et cancer du sein
| Loi du Risque | Loi du côté |
|---|---|
|
Mère cancer du sein : risque double |
La tumeur du même côté que leur mère ou leur sœur |
Score d’Eisinger ou score Inserm
| Situation | Score |
|---|---|
| Mutation de BRCA identifiée dans la famille | 5 |
| Cancer du sein chez femme < 30 ans | 4 |
| Cancer du sein chez femme 30-40 ans | 3 |
| Cancer du sein chez femme 40-50 ans | 2 |
| Cancer du sein chez femme 50-70 ans | 1 |
| Cancer du sein chez l’homme | 4 |
| Cancer ovarien | 3 |
Indication à une consultation d'oncogénétique : score > 5 : formelle ; 3-4 : indication possible ;< 2 : intérêt faible
Suivi d'une personne prédisposée à développer un cancer de l'ovaire
LE CONTEXTE
De 5 à 10 % des cancers épithéliaux de l'ovaire sont associé à une anomalie génétique définie. Dans l'immense majorité des cas il s'agit d'une mutation des gènes BRCA1 et/ou BCRA2 . Cette mutation est associée a une augmentation importante de développer un cancer de l'ovaire.
LES RECOMMANDATIONS ACTUELLES
Le suivi devrait être institué à partir de 35 ans et comprendre, un examen gynécologique biannuel et une échographie endovaginale annuelle.
La prévention est recommandée chez les personnes porteuses de la mutation, ayant le nombre d'enfants souhaité et chez qui existe des arguments cliniques et génétiques évoquant la possibilité d'un syndrome sein-ovaire. Une annexectomie (ablation des ovaires) est à envisager 10 ans plus tôt que l'âge de début du cancer chez l'un des membres de la famille ayant la mutation.
Les autres mesures de prévention seront discutées en réunion de concertation pluridisciplinaire (RCP). Elles portent sur l'opportunité :
- D'un traitement hormonal substitutif (THS)
- D'une FIV avec stimulation ovarienne pour stérilité pour laquelle il n'existe par de contre-indication, en attendant le résultat de la recherche de mutations BRCA . Si la mutation est retrouvée, une ovariectomie sera proposée lorsque le nombre de grossesses attendues est atteint ou après 40 ans. :
Mise à jour
18 mars 2024

