Les différents stades
Pourquoi définir un stade de cancer?
L'évaluation du stade d'évolution d’un cancer demande un ensemble de tests de diagnostic et d'examens permettant d'évaluer le type et l'étendue de la maladie. La détermination précise du stade d'un cancer est l'un des facteurs déterminant pour le choix du type de traitement. Selon les résultats de l'examen clinique et de la biopsie, certains examens d'imagerie médicale peuvent être réalisés. Des analyses sanguines peuvent aussi être effectuées pour permettre de faire un bilan de santé et de détecter si le cancer s'est étendu à certains organes.
Une classification du stade est un code standard international par lequel les équipes de cancérologie décrivent l'extension d'un cancer. Le système appliqué est le système TNM (de l'American Joint Committee on Cancer - AJCC). Les caractéristiques, TNM, attribuées au cancer, peuvent être regroupés en un petit nombre de stades. Les stades sont exprimés par un chiffre allant de 0, pour le stade le moins avancé, à IV pour la forme la plus avancée. Le système TNM se subdivise en deux :
- La stadification clinique pré-thérapeutique, désignée par TNM ou cTNM, c indiquant que le stade a été déterminé par l’examen clinique
- La stadification anatomopathologique et post-chirurgicale désignée par pTNM, p indique que le stade a été donné par l’examen anatomopathologique, par l'examen au microscope de la tumeur qui a été retirée. L’estimation du pronostic est meilleure avec le pTNM qu’avec le cTNM.
Les valeurs de TNM (2017) pour le cancer de l’œsophage
|
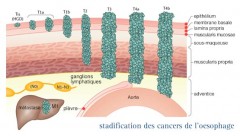
Tumeur T |
Ganglions N |
Métastases M |
|---|---|---|
|
|
|
Stadification (AJCC-UICC 7ème édition)
| Stade | T | N | M |
|---|---|---|---|
| 0 | Tis | N0 | M0 |
| IA IB |
T1 T2 |
||
| IIA IIB |
T3 T1, T2 |
N0 N1 |
|
| IIIA IIIB IIIC |
T3 T1,T2 T3 T4a T4b |
N1 N2 N2 N1, N2 Tout N |
|
| IV | Tout T | Tout N | M1 |
La classification de Siewert (2005) pour les adénocarcinomes
Elle définit trois type de lésions
- Type I : adénocarcinome de l'œsophage distal dont le centre de la tumeur est situé entre 1 cm et 5 cm au dessus de la jonction œsogastrique
- Type II : adénocarcinome à localisation cardiale moyenne dont le centre est situé entre 1 cm au-dessus (limite supérieure) et 2 cm (limite inférieure) au-dessous de la jonction œsogastrique. Cette entité correspond aux adénocarcinomes du cardia vrai
- Type III : lésion du cardia à localisation gastrique prédominante dont le centre tumoral est situé entre 2 cm et 5 cm au-dessous de la jonction œso-gastrique : il s'agit d'un cancer gastrique sous-cardial.
La classification des cancers du cardia est définie en fonction de la distance entre le centre de la tumeur et la ligne Z
- 5 à - 1 cm : Siewert I (adénocarcinome sur endo-brachy-œsophage)
- 1 à + 2 cm : Siewert II (vrai adénocarcinome du cardia)
- 2 à + 5 cm : Siewert III (adénocarcinome gastrique sous-cardial). :
Stadification spécifique aux adénocarcinomes (AJCC 8ème édition - 2017)
| Stade | Tumeur T | Ganglions N | Métastases M |
|---|---|---|---|
| IA | T1a | N0 | M0 |
| IB | T1b | ||
| IIA | T2 | ||
| IIB | T1 T3 |
N1 N0 |
|
| IIIA |
T1 |
N2 |
|
| IIIB |
T2 |
N2 |
|
| IVA |
T4a |
N2 |
|
|
IVB |
Tout T |
Tout N |
M1 |
Au delà de la stadification...
LE GRADE HISTOLOGIQUE
La lettre G (grade) suivie d'un chiffre allant de 1 à 4 indique l’aspect histologique de la tumeur. Ce type de gradation est utilisé pour les cancers invasifs mais pas pour les cancers in situ .
A partir de ces données, les tumeurs sont parfois désignées comme étant bien différenciées, modérément différenciées ou peu différenciées.
Par exemple, les cancers G1 (grade 1) ont des cellules dont l'aspect est relativement normal. Les cellules se multiplient peu (faible nombre de mitoses.)
Les cancers G4, le grade le plus haut, ont des cellules très indifférenciées, un nombre de mitoses est élevé. De nombreuses cellules présentent des anomalies des noyaux cellulaires (ploïdie).
Les cancers G2 ont des caractéristiques intermédiaires entre les grades 1 et 4.
LE RÉACTION DU STROMA
L'apparence des cellules tumorales, l’aspect du stroma (tissu entourant la tumeur) qui est le reflet de la réaction hôte tumeur est décrit. La présence d'un stroma, abondant et fibro-élastique, est considérée comme de bon pronostic. A l'inverse, la présence de zones de nécrose (destruction cellulaire) serait un signe de moins bon pronostic.
LA PLOÏDIE
La ploïdie des cellules cancéreuses se réfère à la quantité d'ADN qu'elles contiennent dans leur noyau. S'il y a une quantité normale d'ADN, les cellules sont dites diploïdes. Si le taux d'ADN est anormal, les cellules sont dites aneuploïdes. Certaines études ont montré que les cancers de l’œsophage aneuploïdes ont tendance à être plus agressifs. Le pourcentage de phase « S » pourrait avoir un intérêt pronostic dans certaines formes de la maladie.
LES AUTRES PARAMÈTRES
L’index Ki-67
Le taux de division des cellules cancéreuses peut aussi être estimé par le test Ki-67. Un index Ki-67 élevé indique que les cellules cancéreuses se divisent rapidement, mais les médecins spécialisés n'accordent pas tous un intérêt à ce test pour déterminer le pronostic de la maladie.
HER2/neu
Dans 15 à 20% des cancers de l’œsophage, principalement de la .jonction gastro-œsophagienne, il existe un taux trop élevé d'une protéine accélératrice de la croissance des cellules, appelée HER2/neu ou C-erbB-2. Cette protéine est mise en évidence à la surface des cellules. En cas de positivité, l'indication d'un traitement ciblant cette protéine sera discutée.
Les nouveaux paramètres en complément du TNM
La recherche du statut MMR tumoral
Il est recommandé d’évaluer systématiquement le statut MMR (MisMatch Repair) tumoral pour tous les adénocarcinomes œsogastriques, dès le diagnostic, quels que soient le stade, l’âge et le contexte familial et personnel du patient dans un but thérapeutique essentiellement et oncogénétique.
La détermination du statut MMR est faite préférentiellement en immunohistochimie des 4 protéines MMR en même temps que la détermination du statut HER2.
En cas de statut dMMR ou de statut MMR indéterminé, le test MSI (instabilité des microsatellites) est utile pour confirmer l’instabilité microsatellitaire.
Maintenant si une immunothérapie ciblée est préconisée pour le traitement d’une lésion MSI non résécable, un statut dMMR et MSI concordant doit être confirmé, en cas de discordance (pMMR/MSI ou dMMR/MSS) un avis de centre expert doit être demandé.
La recherche de la surexpression d’HER2
Pour les patients atteints d’un cancer de l’œsophage avancé, dont l’état général est compatible avec un traitement systémique incluant le trastuzumab, la recherche du statut HER2 sera effectuée et un traitement par le trastuzumab (Herceptin™ ou biosimilaires) en cas de surexpression de HER2 (sera proposé).
Expression de PD-L1 (score CPS et TPS)
Si la possibilité d’utiliser une immunothérapie est envisagée, la détermination du score CPS (Combined Positive Score) sera initiée pour toutes les tumeurs oeso-gastriques non résécables.
Le CPS est le témoin de l’expression de PD-L1 au niveau des cellules tumorales et des cellules immunitaires intra-tumorales (nombre de cellules tumorales PD-L1+ et des cellules immunes PD-L1+ divisé par le nombre total de cellules tumorales viables).
Le score TPS* (Tumor Proportion Score) sera précisé en cas de carcinome épidermoïde, s'il y a une indication pour une immunothérapie par nivolumab.
* Le TPS est l’expression de PD-L1 au niveau des cellules tumorales (% de cellules tumorales PD-L1+ divisé par le nombre total de cellules tumorales viables).
Mise à jour
9 décembre 2023

