Les tumeurs malignes
Des caractéristiques propres
L'ORIGINE
Les tumeurs malignes du sein seraient issues de la multiplication d’une seule cellule issue d’un composant normal du sein et devenue maligne. Ces cellules cancéreuses sont issues soit d'un canal (cancer de type canalaire) soit d'un lobule (cancer de type lobulaire).
LE SIEGE DE LA LESION
Le siège habituel des cancers du sein est le quadrant supéro- externe dans environ 40 % des cas, suivi de la région centrale. Les autres quadrants sont moins souvent atteints. Cette topographie s’explique par la quantité de tissu glandulaire toujours plus présent dans la partie centrale et supéro- externe.
SON ÉVOLUTION
Par rapport aux tumeurs bénignes, les cancers se présentent sous la forme d’une masse mal limitée avec des prolongements. C’est cette caractéristique qui est à l’origine du nom « cancer » qui veut dire « crabe » en latin.
Surtout le cancer se distingue par son évolution. Il augmente de volume de façon plus rapide qu’une tumeur bénigne. Non traité, le cancer se propage aux ganglions lymphatiques, aux organes de voisinage, ainsi qu’aux organes à distance.
L'évolution d'une tumeur
De 5 à 10 ans entre les premières cellules cancéreuses et la découverte d'une tumeur de 0,5 et 1,5 cm
Temps de doublement de taille d’une tumeur maligne : 3 mois
1 gramme de tumeur c'est déjà un milliard de cellules !
Quelques valeurs pour expliquer l'évolution de la maladie
|
Cancer du sein |
Survie à 5 ans |
Survie à 5 ans |
Rechutes tardives à |
Temps de doublement de la tumeur primitive en jours |
Doublement de volume jusqu’au diagnostic |
Temps de passage à T1 lors du diagnostic (années) |
|---|---|---|---|---|---|---|
|
Globalement |
– |
– |
– |
– |
33 |
– |
|
Récepteurs hormonaux RH+ |
99 |
19 |
13–34 |
111–398 |
– |
10–36 |
|
Triple négatif |
76 |
14 |
9 |
77–177 |
– |
7–16 |
Klein, C.A. Cancer progression and the invisible phase of metastatic colonization. Nat Rev Cancer 20, 681–694 (2020)
LA DISSÉMINATION
LA DISSÈMINATION AU-DELÀ DU SEIN
L'évènement le plus fâcheux au cours de l'évolution d'un cancer du sein, est la survenue de métastases ou dissémination des cellules tumorales au-delà de la glande mammaire.
L'ATTEINTE DES GANGLIONS
Où ?
C’est surtout sous le bras (creux axillaire ou aisselle) que peuvent se retrouver, à la palpation, les ganglions, au cours de l’évolution de la maladie. Il est, aussi, fréquent de retrouver des petits ganglions dans l’aisselle sans que cela soit un signe de cancer. Même lorsque l’on palpe des ganglions de la taille d’une noisette (~1 cm) chez une femme atteinte d’un cancer du sein, ceux-ci peuvent ne pas être des ganglions cancéreux, mais seulement des ganglions inflammatoires. Seule l’analyse au microscope, du ou des ganglions, peut permettre de savoir s’ils sont touchés par le cancer. C’est pourquoi lors de l’intervention pour un cancer du sein, les ganglions axillaires sont enlevés (curage axillaire) et analysés.
Sa signification…
L’atteinte des ganglions lymphatiques signifie que certaines cellules cancéreuses ont eu la capacité de sortir de la glande mammaire pour former d'autres colonies tumorales en dehors du sein.
Il existe donc un risque que d'autres cellules aient suivi le même processus pour aller dans d'autres organes du corps. C'est pourquoi il est important de déterminer si le cancer du sein s'est étendu aux ganglions lymphatiques axillaires afin de mettre sur pied le meilleur traitement.
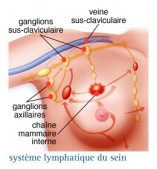
Quels sont ganglions concernés ?
Les ganglions du creux axillaire peuvent être palpés
La chaîne mammaire interne est derrière le sternum; elle ne peut pas être palpée
Le creux sus claviculaire peut être palpé, mais les ganglions y sont plus rarement retrouvés
Les métastases
Elles se font par migration des cellules tumorales soit par les vaisseaux lymphatiques soit par les vaisseaux sanguins. Les organes le plus fréquemment touchés sont l'os, le cerveau, le foie et le poumon.
| Le risque de métastase est plus élevé... |
|---|
|
LES MÉTASTASES CÉRÉBRALES
C'EST RELATIVEMENT FREQUENT CE QUI IMPLIQUE DE LES RECHERCHER...
Lors du diagnostic de la maladie, au stade non métastatique, le risque de développer des métastases cérébrales est de 5 à 10 %. Dans un peu plus de 1 % des cas, elles inaugurent la maladie métastatique.
Les facteurs de risque
De nombreux travaux ont montré que le risque de développer des métastases cérébrales était plus élevé dans les cas suivants :
- Le jeune âge (avant 40 ans)
- Une atteinte ganglionnaire
- Une tumeur de grade 3
- Les tumeurs n’exprimant pas les récepteurs hormonaux
- Le phénotype basal, triple négatif (HER2, non surexprimé, récepteurs des estrogènes et récepteurs de la progestérone négatifs non exprimés)
- Les tumeurs exprimant HER2
- L'existence d'une maladie extra-cérébrale étendue (plus de deux sites métastatiques)
Selon le type biomoléculaire de la maladie
Le risque est plus élevé pour les tumeurs exprimant HER2 (25 à 49 %) et les cancers dits "triple négatifs" (25 à 46 %).
Il est plus faible pour les tumeurs de type luminales B (HER2 non surexprimé, récepteurs des estrogènes et de la progestérone exprimés, indice de prolifération élevé), 10 % et luminales A, de l'ordre de 7 %..
Le délai de survenue des métastases cérébrales par rapport au diagnostic initial
Il est différent pour les tumeurs respectivement triple négatives (28 mois), HER2 (36 mois), luminales B (47 mois) et luminales A (54 mois).
LE PRONOSTIC
Les durées médianes de survie, selon les données de la littérature, vont de 3 à 25 mois à partir du diagnostic de métastase(s) cérébrale(s) : 7,3 mois pour les tumeurs triples négatives, 18 mois pour les tumeurs exprimant HER2, 10 mois pour les tumeurs luminales A et 23 mois pour les tumeurs luminales B.
Mise à jour
29 juillet 2022

