La stadification
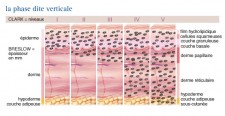
Classifications de Clark et de Breslow
Contrairement à la plupart des autres cancers, la stadification du mélanome est effectuée à partir de la pièce d’exérèse après son examen au laboratoire. L’étude histologique permet aussi, en fonction de la profondeur de la lésion, de définir une classification de valeur pronostique.
Pour le mélanome, six classifications internationales ont été successivement utilisées qui ont tous des avantages et parfois des inconvénients.
LE NIVEAU DE CLARK ET MIHM
Le niveau d'invasion est basé sur le concept de franchissement de barrières anatomiques. Cette classification permet de définir 5 stades, dénommés Clark avec un chiffre allant de I à V :
- Niveau I : les cellules malignes se trouvent au-dessus de la couche basale (mélanome in situ).
- Niveau II : les cellules malignes ont envahi le derme papillaire mais pas le derme réticulaire.
- Niveau III : la tumeur s'est étendue à la zone entre le derme papillaire et le derme réticulaire, où commence la formation des faisceaux collagènes.
- Niveau IV : des cellules malignes sont présentes entre les faisceaux collagènes du derme réticulaire.
- Niveau V : des cellules malignes ont atteint les tissus sous-cutanés
LA CLASSIFICATION DE BRESLOW
Elle a été proposée par Alexander Breslow (1928 - 1980), anatomopathologiste américain. Elle est basée sur l’épaisseur de la tumeur, en millimètres. La mesure est effectuée à l'oculaire micrométrique et se fait à partir d’une coupe histologique standard.
Elle mesure l’épaisseur maximum comprise entre les cellules superficielles de la couche granuleuse épidermique et la base de la tumeur (cellule maligne la plus profonde).
- < 0,75 mm
- 0,76 à 1,50 mm
- 1,51 à 4 mm
- > 4 mm
L'épaisseur est une appréciation indirecte de la masse de la tumeur. Il existe une corrélation presque linéaire entre épaisseur et le pronostic.
CLASSIFICATION T.N.M. - Principe
Une classification du stade est un code standard international par lequel les équipes de cancérologie décrivent l'extension d'un cancer.
Le système appliqué est le système T.N.M. (de l'American Joint Committee on Cancer).
Les caractéristiques, T.N.M., attribuées au cancer, peuvent être regroupées en un petit nombre de stades. Les stades sont exprimés par un chiffre, allant de 0, pour le stade le moins avancé, à IV pour le plus avancé. Les deux systèmes « TNM » .
Dans le cas du mélanome, c'est la stadification anatomopathologique et post chirurgicale désignée par pTNM (p indique que le stade a été donné par l’examen anatomopathologique après examen au microscope) qui est utilisée.
Les "valeurs" de T,N,M ont été précisées par la classification pTNM de l’UICC et de l’AJCC, 8ème édition. Elles sont présentées dans le tableau ci-dessous.
LA STADIFICATION SELON LA CLASSIFICATION DE L’AJCC 2017
La 8 ème édition de l' AJCC prend en considération le statut du ganglion sentinelle en plus d’autres facteurs de pronostic, tels que l’épaisseur de la tumeur primaire mesurée en millimètres et l’ulcération. Une attention particulière est, également, donnée à l’invasion métastatique des ganglions régionaux. Ainsi, le nombre de ganglions lymphatiques atteints et la présence de micro-métastases dans le ganglion sentinelle sont considérés dans la classification. Pour les stades IV, la classification se base sur deux paramètres reflétant l’agressivité de la maladie, le type de métastases à distance et l'élévation de taux de LDH dans le sang (marqueur de la masse tumorale).
| Tumeur T | Ganglions N | Métastases M |
|---|---|---|
|
T1 : Breslow < 1 mm |
N0 pas de ganglions envahis |
M1a : métastase(s) cutanée(s), sous-cutanée(s), ganglionnaire(s) à distance 1 : t LDH élevée |
La stadification pathologique
Elle est effectuée à partir de l’étude des tissus au microscope. C’est pour cette raison que la valeur de T est précédée de p qui correspond à une classification à partir des données de laboratoire sur la pièce opératoire enlevée lors de l’exérèse :
- pT1 mélanome de < 0,75 mm d’épaisseur ou à une tumeur localisée dans le derme papillaire
- pT2 tumeur mesurant de 0,75 à 1,50 mm d’épaisseur ou une tumeur envahissant jusqu’à la jonction réticulo-papillaire du derme
- pT3 lésion de 1,50 à 4 mm ou envahissement du derme réticulaire. Ce niveau est, lui-même, sous divisé en deux.
- pT3a : tumeur de 1,50 à 3 mm d’épaisseur
- pT3b : tumeur de 3 à 4 mm d’épaisseur
- pT4 : mélanomes de plus de 4 mm d’épaisseur ou envahissement du tissu sous-cutané ou au-delà. Dans ce cas, il existe des lésions satellites situées dans les 2 cm autour de la tumeur initiale. Pour ce stade, deux sous stades sont définis.
- pT4a : tumeur de plus de 4 mm d’épaisseur, envahissement du tissu sous-cutané ou plus
- pT4b : présence de nodules satellites moins de 2 cm autour de la tumeur
La classification en stades pronostiques (AJCC 2017)
|
Mélanome localisé |
Métastases régionales |
Métastases à distance |
|---|---|---|
|
Stade 0 : Tis
|
Stade IIC : T0, N1b et N1c |
Stade IV : tout T ; tout N |
Au delà de la stadification...
LE GRADE DE LA TUMEUR
Le principe
Le médecin anatomopathologiste examine les tissus prélevés au microscope (examen histologique) et leur attribue un grade pathologique. Le grade pathologique aide à préciser la stratégie thérapeutique et d’évaluer le pronostic de la maladie. Plus les tumeurs sont indifférenciées, c’est à dire différent des structures normales, plus elles sont agressives. A l’inverse, plus une tumeur est différenciée, c’est à dire proche de la structure normale, plus son évolution est favorable.
Les grades
La lettre G (grade) suivie d’un chiffre allant de 1 à 4 indique l’aspect histologique de la tumeur.
Ce type de gradation est utilisé pour les mélanomes invasifs. Les mélanomes sont parfois désignés comme étant bien différenciés, modérément différenciés ou peu différenciés. Par exemple, les mélanomes G1 ou grade 1, ont des cellules dont l’aspect est relativement normal. Les cellules se multiplient peu (faible nombre de mitoses.)
Les mélanomes G4, le grade le plus haut, ont des cellules très indifférenciées, un nombre de mitoses est élevé. De nombreuses cellules présentent des anomalies des noyaux cellulaires (ploïdie).
Les mélanomes G2 et G3 ont des caractéristiques intermédiaires entre les grades 1 et 4.
LA RÉACTION DU « STROMA »
En plus de l’apparence des cellules tumorales, l’aspect du stroma (tissu entourant la tumeur) qui est le reflet de la réaction hôte tumeur est décrit. Un stroma abondant et fibroélastique sont en général de bon pronostic. A l’inverse, la présence de zones de nécrose (destruction cellulaire) serait un signe de moins bon pronostic.
LA PLOÏDIE
La ploïdie des cellules cancéreuses se réfère à la quantité d’ADN qu’elles contiennent dans leur noyau. S’il y a une quantité normale d’ADN, les cellules sont dites diploïdes. Si le taux d’ADN est anormal, les cellules sont dites aneuploïdes. Il n’y a pas de consensus sur l’intérêt pronostic de ce paramètre.
INDEX KI-67
Le taux de division des cellules cancéreuses peut aussi être estimé par le test Ki-67. Un index Ki-67 élevé indique que les cellules cancéreuses se divisent rapidement.
LES MOLÉCULES D’ADHÉSION
L’étude des molécules qui assurent la jonction entre les cellules (molécules d’adhésion) pourrait être un bon critère pour identifier les tumeurs à haut risque de dissémination.
Vers une classification biomoléculaire des mélanomes de la peau...
De très nombreux travaux de biologie moléculaire et de recherche translationnelle ont mis en évidence de nombreuses anomalies génétiques affectant les cellules tumorales des mélanomes. Actuellement, les résultats sont établis pour les anomalies génétiques suivantes :
| Mutations d'oncogènes | Gènes suppresseurs de tumeur | Autres anomalies génétiques |
|---|---|---|
|
BRAF (50 % de mutations) |
CDKN2A (30–70 % de délétions, mutations, ou d'inactivations) |
C CND1 (6–44 % amplifiés) |
A terme, cela devrait déboucher sur une classification biomoléculaire des mélanomes et vers une personnalisation plus poussée des traitements ciblant des anomalies génétiques spécifiques.
Mise à jour
17 avril 2020

